При горении водорода H2 в кислороде образуется вода.Напишите уравнение реакции. Горение водорода Формула для горения воды
T =1.5 ·10 7 K. Для каждой реакции приведено энерговыделение (энергия реакции Q).
Первая реакция в цепочке - взаимодействие двух ядер водорода с образованием дейтрона, позитрона и нейтрино. Эта реакция происходит в результате слабого взаимодействия и является определяющей в скорости всей pp-цепочки (t = 5.8 ·10 9 лет). На втором этапе в результате взаимодействия образовавшегося дейтрона с водородом происходит образование изотопа 3 He с испусканием -кванта. Далее может реализоваться одна из двух возможностей. С вероятностью 69% происходит реакция:
дающей поток высокоэнергичных нейтрино, доступный для регистрации. Полная энергия (суммарная энергия реакции Q), выделяющаяся в результате синтеза изотопа 4 He из 4 протонов, составляет 24.7 МэВ - для цепочек ppI, ppIII и 25.7 МэВ для цепочки ppII. Образующиеся при синтезе позитроны аннигилируют, увеличивая энерговыделение для всех цепочек до 26.7 МэВ.
В табл. 8 приведены значения коэффициента S ij при E = 0 для некоторых реакций pp - цикла и неопределенности оценок величин соответствующих коэффициентов.
Таблица 8
Значение величин коэффициента S ij в реакциях pp-цикла
Значения S ij , МэВ·мб |
|||
p + p → d + e + + ν |
|||
| 3 He + 3 He → 4 He + 2p |
|||
3 He + 4 He → 7 Be + γ |
|||
7 Be + p → 8 B + γ |
Значения S ij и их неопределенности, приведенные
в таблице, позволяют получить представление о сложности расчетов ядерных реакций
в звездах и точности, достигнутой на сегодняшний день.
Водородный цикл может начинаться также с реакции:
В звездах с массой большей, чем у Солнца, pp - цепочка не
является главным источником энергии.
Вещество звезд второго поколения наряду с водородом и гелием
содержит более тяжелые элементы, образующиеся в реакциях горения водорода и
гелия, и, в частности, азот, углерод, кислород, неон и другие. Эти элементы
играют роль катализаторов в реакциях горения водорода.
Когда температура в центре звезды приближается к 20 млнK, в
звездах начинается цепочка ядерных реакций, в ходе которых ядра углерода
испытывают ряд последовательных превращений, а из водорода образуется гелий. Эта
цепочка реакций называется CNO - циклом.
Водорода составляет примерно 140 МДж/кг (верхняя) или 120 МДж/кг (нижняя), что в несколько раз превышает удельную теплоту сгорания углеводородных топлив (для метана - около 50 МДж/кг).
Гремучий газ самовоспламеняется при атмосферном давлении и температуре 510 °C. При комнатной температуре в отсутствие источников зажигания (искра, открытое пламя) гремучий газ может храниться неограниченно долго, однако он способен взорваться от самого слабого источника, так как для инициирования взрыва достаточно искры с энергией 17 микроджоулей . С учётом того, что водород обладает способностью проникать через стенки сосудов, в которых он хранится, например, диффундировать сквозь металлические стенки газового баллона, и не обладает никаким запахом, при работе с ним следует быть чрезвычайно осторожным.
Получение
Применение
Кривая зависимости между критическими давлением и температурой, при которых происходит самовоспламенение смеси, имеет характерную Z-образную форму, как показано на рисунке. Нижняя, средняя и верхняя ветви этой кривой называются соответственно первым, вторым и третьим пределами воспламенения. Если рассматриваются только первые два предела, то кривая имеет форму полуострова, и традиционно этот рисунок называется полуостровом воспламенения.
Спорные теории
В 1960-е года американский инженер Уильям Роудс (William Rhodes) якобы открыл «новую форму» воды, коммерциализированную Юллом Брауном (Yull Brown), болгарским физиком, эмигрировавшим в Австралию. «Брауновский газ», то есть фактически смесь кислорода и водорода, получаемая в аппарате электролиза воды, объявлялся способным очищать радиоактивные отходы, гореть как топливо, расслаблять мышцы и стимулировать проращивание семян . Впоследствии итальянский физик Руджеро Сантилли (en:Ruggero Santilli) выдвинул гипотезу, утверждающую существование новой формы воды в виде «газа HHO», то есть химической структуры вида (H × H - O), где «×» представляет гипотетическую магнекулярную связь, а «-» - обычную ковалентную связь. Статья Сантилли, опубликованная в авторитетном реферируемом журнале International Journal of Hydrogen Energy , вызвала жёсткую критику со стороны коллег, назвавших утверждения Сантилли псевдонаучными , однако некоторые другие учёные выступили в поддержку Сантилли .
Примечания
- , с. 85,196.
- , с. 311.
- Konnov A. A. Remaining uncertainties in the kinetic mechanism of hydrogen combustion // Combustion and Flame . - Elsevier, 2008. - Vol. 152, № 4 . - P. 507–528. - DOI :10.1016/j.combustflame.2007.10.024 .
- Shimizu K., Hibi A., Koshi M., Morii Y., Tsuboi N. Updated Kinetic Mechanism for High-Pressure Hydrogen Combustion // Journal of Propulsion and Power. - American Institute of Aeronautics and Astronautics, 2011. - Vol. 27, № 2 . - P. 383–395. - DOI :10.2514/1.48553 .
- Burke M. P., Chaos M., Ju Y., Dryer F. L., Klippenstein S. J. Comprehensive H 2 /O 2 kinetic model for high-pressure combustion // International Journal of Chemical Kinetics. - Wiley Periodicals, 2012. - Vol. 44, № 7 . - P. 444–474. - DOI :10.1002/kin.20603 .
- , с. 35.
- Ball, Philip. Nuclear waste gets star attention (англ.) // Nature : journal. - 2006. - ISSN 1744-7933 . - DOI :10.1038/news060731-13 .
- Ruggero Maria Santilli. A new gaseous and combustible form of water (англ.) // International Journal of Hydrogen Energy : journal. - 2006. - Vol. 31 , no. 9 . - P. 1113-1128 . - DOI :10.1016/j.ijhydene.2005.11.006 .
- J. M. Calo. Comments on "A new gaseous and combustible form of water" by R.M. Santilli (Int. J. Hydrogen Energy 2006: 31(9), 1113–1128) (англ.) // International Journal of Hydrogen Energy : journal. - 2006. - 3 November (vol. 32 , no. 9 ). - P. 1309-1312 . -
Реакция горения водорода может быть описана уравнением

Реакции горения водорода и оксида углерода во многом похожи. Обе они являются сильными экзотермическими реакциями с тепловыми эффектами одного порядка. Стехиометрические соотношения между количествами взаимодействующих веществ в уравнениях реакций (1.11) и (1.1) одинаковы. Поэтому качественная оценка влияния изменения параметров системы на протекание реакций горения водорода и оксида углерода при помощи правила фаз Гиббса и принципа Ле Шателье приводит к одинаковым выводам.
Протекание реакции (1.11) в направлении диссоциации H 2 O становится возможным в условиях, когда
Из уравнения (1.12) формулу для определения константы равновесия реакции (1.11) можно получить в виде
Результаты расчета константы равновесия реакции (1.11) при различных температурах представлены в таблице 1.2.
Таблица 1.2 – Значения константы равновесия реакции (1.11) при различных температурах
Анализ данных таблицы 1.2 показывает, что при температурах до 2000К константа равновесия реакции (1.11) также имеет очень высокие значения. Это позволяет в широком диапазоне температур считать реакцию горения водорода практически не обратимой. Диссоциация H 2 O становится возможной только при малых концентрациях водорода и кислорода или очень низком давления смеси газов P общ.
Окислительный потенциал газовой смеси при протекании реакции (1.11) также может быть охарактеризован величиной равновесного парциального давления кислорода

Анализ уравнения (1.15) позволяет сделать следующие выводы:
- Для газовой смеси с постоянным соотношением между концентрациями H 2 O и H 2 величина равновесного парциального давления кислорода зависит только от температуры.
- При повышении температуры численное значение константы равновесия реакции (1.11) уменьшается, а окислительный потенциал газовой смеси увеличивается.
- При неизменной температуре величина равновесного парциального давления кислорода определяется соотношением между объемными концентрациями H 2 O и H 2 в смеси. Окислительный потенциал газовой смеси повышается при увеличении (%H 2 O) и уменьшается при увеличении (%H 2).
Между реакциями (1.11) и (1.1) имеются также и некоторые различия. Так как ![]() , при повышении температуры константа равновесия реакции горения оксида углерода уменьшается быстрее, чем константа равновесия реакции горения водорода.
, при повышении температуры константа равновесия реакции горения оксида углерода уменьшается быстрее, чем константа равновесия реакции горения водорода.
Расчеты показывают, что при температуре 1083К ![]() . Это означает, что при соблюдении условия
. Это означает, что при соблюдении условия
окислительный потенциал газовой смеси при протекании реакций горения оксида углерода и водорода будет одинаковым.
Помогите пожалуйста. Задание 1: при горение водорода H2 в кислороде образуется вода. Напишите уравнение реакции. Задание 2: Сероуглерод CS2 - летучаяядовитая жидкость,используемая в производстве некоторых искусственных волокон. Приего горение в кислороде образуется сернистый и углекислый газы. Напишите уравнение уравнение этой реакции. Зарание всех благодарю:)
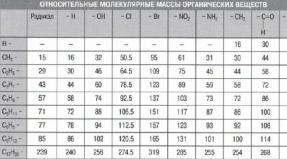
1. Напишите уравнение реакции горения пропилена и укажите сумму коэффициентов в левой части уравнения.2. Напишите уравнение реакции окисления толуола и укажите сумму коэффициентов в правой части уравнения
3. Вычислите и укажите объем углекислого газа (н.у.), который образовался вследствие сжигания 0,5 моль етину.
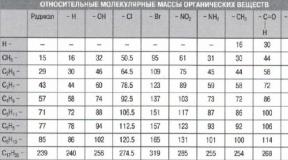
4. Добавить относительную молекулярную массу органического продукта реакции полного бромирования пропина
5. Вычислите и укажите объем кислорода (н.у.), который потратится на сжигание 12 м3 етину
6. Добавить объем и название продукта, образующегося при гидрировании 0,8 м3 етину водородом, объем которого 0,4 м3.
7. Добавить какую массу хлора может присоединить 0,1 моль етину
8. Определите неизвестный углеводород в реакции
2CXHY +15 O2 = 10CO2 +10 H2O
9. Добавить формулу углеводорода ряда ряда ацетилена, плотность по гелием которого равна 10
10. Вычислите и укажите объем кислорода (н.у.), который потратится на сжигание 30м3 пропина (н.у.)
11. Напишите уравнения реакций, с которыми можно осуществить следующие преобразования:
CaC2 = C2H2 = C6H6 = C6H5NO2
Добавить сумму коэффициентов во всех уравнениях реакций
12. Напишите уравнения реакций, с которыми можно осуществить следующие преобразования:
Кальций оксид = кальций карбид = ацетилен = бензин = хлоробензен
Добавить сумму коэффициентов во всех уравнениях реакции
кислороде. Продукт - оксид фосфора (V)
3.Напишите уравнение реакций горения угля (углерода) . Продукт - оксид углерода (IV)
4. напишите уравнение реакции натрия с кислородом
5.Напишите уравнение реакций окисления сульфида железа (II) с кислородом
6.Что получится при взаимодействий алюминия с иодом
Помогите пожалуйста решить: (1) Напишите уравнения реакций между кислородом и следующими веществами: 1)натрием 2)кремнием 3) этиленом, формулакоторого: C2H4
(2)Напишите уравнения реакций, при помощи которых можно осуществить превращение:
C -> CO2 -> CaCO3 -> CaO
(3)Допишите уравнения реакций:
CuO + ... = Cu + H2O
H2 + Ci2 = .....
(4)Сколько литров сероводорода получится при взаимодействии 2 литров водорода с серой?
1) определите, с каким из приведенных веществ реагируют как вода, так и гидроксид калия: Fe(OH)2, SO2, NaCL. Напишите уравнения реакций и укажитеназвания образующихся веществ.
2)Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Ca - Ca(OH)2 - CaCO3 - CO2
3) В воде объемом 500 см в кубе растворили 70 г сахара. Вычислите массовую долю сахара в полученном растворе.
* Рассчитайте массу осадка, который образуется при взаимодействии 11,7 г хлорида натрия с нитратом серебра.
Помогите пожалуйста это очень сроч
заранее спс.
Одной из актуальных проблем является загрязнение окружающей среды и ограниченность энергетических ресурсов органического происхождения. Многообещающим способом решения этих проблем является использование водорода в качестве источника энергии. В статье рассмотрим вопрос горения водорода, температуру и химию этого процесса.
Что такое водород?
Прежде чем рассматривать вопрос, какая температура сгорания водорода, необходимо вспомнить, что собой представляет это вещество.
Водород — это самый легкий химический элемент, состоящий всего из одного протона и одного электрона. При нормальных условиях (давление 1 атм., температура 0 o C) он присутствует в газообразном состоянии. Его молекула (H 2) образована 2 атомами этого химического элемента. Водород является 3-м по распространенности элементом на нашей планете, и 1-м во Вселенной (около 90 % всей материи).
Водородный газ (H 2) не имеет запаха, вкуса и цвета. Он не токсичен, однако, когда содержание его в атмосферном воздухе составляет несколько процентов, то человек может испытывать удушье, по причине недостатка кислорода.
Любопытно отметить, что хотя с химической точки зрения все молекула H 2 идентичны, физические свойства их несколько отличаются. Дело все в ориентации спинов электронов (они ответственны за появление магнитного момента), которые могут быть параллельными и антипараллельными, такую молекулу называют орто- и параводородом, соответственно.
Химическая реакция горения

Рассматривая вопрос, температуры горения водорода с кислородом, приведем химическую реакцию, которая описывает этот процесс: 2H 2 + O 2 => 2H 2 O. То есть в реакции участвуют 3 молекулы (две водорода и одна кислорода), а продуктом являются две молекулы воды. Эта реакция описывает горение с химической точки зрения, и по ней можно судить, что после ее прохождения остается только чистая вода, которая не загрязняет окружающую среду, как это происходит при сгорании органического топлива (бензина, спирта).
С другой стороны, эта реакция является экзотермической, то есть помимо воды она выделяет некоторое количества тепла, которое можно использовать для приведения в движение машин и ракет, а также для его перевода в другие источники энергии, например, в электричество.
Механизм процесса горения водорода

Описанная в предыдущем пункте химическая реакция известна любому школьнику старших классов, однако она является очень грубым описанием того процесса, который происходит в действительности. Отметим, что до середины прошлого века человечество не знало, как происходит горение водорода в воздухе, а в 1956 году за ее изучение была присуждена Нобелевская премия по химии.
В действительности, если столкнуть молекулы O 2 и H 2 , то никакой реакции не произойдет. Обе молекулы являются достаточно устойчивыми. Чтобы горение происходило, и образовывалась вода, необходимо существование свободных радикалов. В частности, атомов H, O и групп OH. Ниже приводится последовательность реакций, которые происходят в действительности при горении водорода:
- H + O 2 => OH + O;
- OH + H 2 => H 2 O + H;
- O + H 2 = OH + H.
Что видно из этих реакций? При горении водорода образуется вода, да, верно, но происходит это только, когда группа из двух атомов OH встречается с молекулой H 2 . Кроме того, все реакции происходят с образованием свободных радикалов, это означает, что запускается процесс самоподдержания горения.
Таким образом, ключевой момент в запуске этой реакции заключается в образовании радикалов. Они появляются, если поднести к кислород-водородной смеси горящую спичку, либо если нагреть эту смесь выше определенной температуры.
Инициация реакции
Как было отмечено, сделать это можно двумя способами:
- С помощью искры, которая должна предоставить всего 0,02 мДж теплоты. Это очень маленькое значение энергии, для сравнения скажем, что аналогичное значение для бензиновой смеси составляет 0,24 мДж, а для метановой — 0,29 мДж. С уменьшением давления энергия инициации реакции растет. Так, при 2 кПа она составляет уже 0,56 мДж. В любом случае, это очень маленькие значения, поэтому водород-кислородная смесь считается легко воспламеняющейся.
- С помощью температуры. То есть кислород-водородную смесь можно просто нагревать, и выше некоторой температуры она сама воспламенится. Когда это произойдет, зависит от давления и процентного соотношения газов. В широком интервале концентраций при атмосферном давлении реакция самовозгорания происходит при температурах выше 773-850 К, то есть выше 500-577 o C. Это достаточно высокие значения по сравнению с бензиновой смесью, которая начинает самовоспламеняться уже при температурах ниже 300 o C.
Процентное содержание газов в горючей смеси

Говоря о температуре горения водорода в воздухе, следует отметить, что не всякая смесь этих газов будет вступать в рассматриваемый процесс. Экспериментально установлено, что если количество кислорода меньше 6% по объему, либо если количество водорода меньше 4% по объему, то никакой реакции не будет. Тем не менее, пределы существования горючей смеси являются достаточно широкими. Для воздуха процентное содержание водорода может составлять от 4,1 % до 74,8 %. Отметим, что верхнее значение как раз соответствует необходимому минимуму по кислороду.
Если же рассматривается чистая кислород-водородная смесь, то здесь пределы еще шире: 4,1-94 %.
Уменьшение давления газов приводит к сокращению указанных пределов (нижняя граница поднимается, верхняя — опускается).
Также важно понимать, что в процессе горения водорода в воздухе (кислороде), возникающие продукты реакции (вода) приводят к уменьшению концентрации реагентов, что может привести к прекращению химического процесса.
Безопасность горения

Это важная характеристика воспламеняющейся смеси, поскольку она позволяет судить о том, происходит реакция спокойно, и можно ее контролировать, либо процесс имеет взрывной характер. От чего зависит скорость горения? Конечно же, от концентрации реагентов, от давления, а также от количества энергии "затравки".
К большому сожалению, водород в широком интервале концентраций способен к взрывному горению. В литературе приводятся следующие цифры: 18,5-59 % водорода в воздушной смеси. Причем на краях этого предела в результате детонации выделяется наибольшее количество энергии на единицу объема.
Отмеченный характер горения представляет большую проблему для использования этой реакции в качестве контролируемого источника энергии.
Температура реакции горения
Теперь мы подошли непосредственно к ответу на вопрос, какая низшая температура сгорания водорода. Она составляет 2321 К или 2048 o C для смеси с 19,6 % H 2 . То есть температура горения водорода в воздухе выше 2000 o C (для других концентраций она может достигать 2500 o C), и в сравнении с бензиновой смесью — это огромная цифра (для бензина около 800 o C). Если сжигать водород в чистом кислороде, то температура пламени будет еще выше (до 2800 o C).
Столь высокая температура пламени представляет еще одну проблему в использовании этой реакции в качестве источника энергии, поскольку не существует в настоящее время сплавов, которые могли бы работать длительное время в таких экстремальных условиях.
Конечно, эта проблема решается, если использовать хорошо продуманную систему охлаждения камеры, где происходит горение водорода.
Количество выделяемой теплоты
В рамках вопроса температуры горения водорода любопытно также привести данные о количестве энергии, которая выделяется во время этой реакции. Для разных условий и составов горючей смеси получили значения от 119 МДж/кг до 141 МДж/кг. Чтобы понять, насколько это много, отметим, что аналогичное значение для бензиновой смеси составляет около 40 МДж/кг.
Энергетический выход водородной смеси намного выше, чем для бензина, что является огромным плюсом для ее применения в качестве топлива для двигателей внутреннего сгорания. Однако, и здесь не все так просто. Все дело в плотности водорода, она слишком низка при атмосферном давлении. Так, 1 м 3 этого газа весит всего 90 грамм. Если сжечь этот 1 м 3 H 2 , то выделится около 10-11 МДж теплоты, что уже в 4 раза меньше, чем при сжигании 1 кг бензина (чуть больше 1 литра).
Приведенные цифры говорят о том, что для использования реакции горения водорода необходимо научиться хранить этот газ в баллонах с высоким давлением, что создает уже дополнительные сложности, как в технологическом вопросе, так и с точки зрения безопасности.
Применение водородной горючей смеси в технике: проблемы

Сразу необходимо сказать, что в настоящее время водородная горючая смесь уже используется в некоторых сферах человеческой деятельности. Например, в качестве дополнительного топлива для космических ракет, в качестве источников для выработки электрической энергии, а также в экспериментальных моделях современных автомобилей. Однако масштабы этого применения являются мизерными, по сравнению с таковыми для органического топлива и, как правило, носят экспериментальных характер. Причиной этому являются не только трудности в контроле самой реакции горения, но также в хранении, транспортировке и добыче H 2 .
Водород на Земле практически не существует в чистом виде, поэтому его необходимо получать из различных соединений. Например, из воды. Это достаточно популярный способ в настоящее время, который осуществляется с помощью пропускания электрического тока через H 2 O. Вся проблема заключается в том, что при этом расходуется больше энергии, чем потом можно получить путем сжигания H 2 .
Еще одна важная проблема — транспортировка и хранение водорода. Дело в том, что этот газ, ввиду маленьких размеров его молекул, способен "вылетать" из любых контейнеров. Кроме того, попадая в металлическую решетку сплавов, он вызывает их охрупчивание. Поэтому наиболее эффективным способом хранения H 2 является использование атомов углерода, способных прочно связывать "неуловимый" газ.

Таким образом, применение водорода в качестве топлива в более-менее широких масштабах возможно, только если его использовать в качестве "сохранения" электричества (например, переводить ветровую и солнечную энергию в водород с помощью электролиза воды), либо если научиться доставлять H 2 из космоса (где его очень много) на Землю.